definícia periodického práva
 The periodický zákon je on založenie periodickej tabuľky prvkovako univerzálna schéma, ktorá organizuje, klasifikuje a distribuuje rôzne existujúce chemické prvky vo vzťahu k ich vlastnostiam a vlastnostiam.
The periodický zákon je on založenie periodickej tabuľky prvkovako univerzálna schéma, ktorá organizuje, klasifikuje a distribuuje rôzne existujúce chemické prvky vo vzťahu k ich vlastnostiam a vlastnostiam.
Základ, na ktorom sedí periodická tabuľka prvkov
Medzitým periodický zákon ustanovuje, že fyzikálne a chemické vlastnosti vyššie uvedených prvkov sú náchylné k systematickému opakovaniu, keď sa zvyšuje atómový počet prvkov.
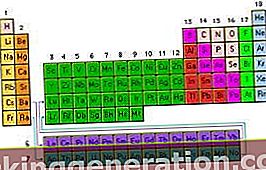
Periodická tabuľka: organizácia chemických prvkov vo vzrastajúcom poradí podľa počtu atómov, ktoré každý z nich má
Tak slávna tabuľka prvkov, ktoré študujeme v škole, na predmetoch fyzika a chémia, je schéma, ktorá sa zaoberá usporiadaním chemických prvkov podľa ich narastajúceho poradia z hľadiska počtu atómov.
Vertikálne stĺpce tabuľky sa nazývajú skupiny a obsahujú prvky s rovnakou atómovou valenciou, a preto majú podobné vlastnosti, zatiaľ čo vodorovné riadky, ktoré sa nazývajú bodky, zoskupujú prvky s rôznymi vlastnosťami, ale majú podobné hmotnosti.
Ako boli tieto vedomosti rozšírené: konkrétne a postupné udalosti
Je potrebné poznamenať, že všetky tieto pojmy, ktoré sú vlastné fyzike a chémii, sa vyvíjali postupne a progresívne v priebehu devätnásteho storočia.
Musíme povedať, že niektoré prvky ako striebro (Ag), zlato (Au), meď (Cu), olovo (Pb) a ortuť (Hg) už od staroveku disponovali dokonalými poznatkami, k prvému vedeckému objavu prvku došlo v priebehu sedemnásteho storočia, keď alchymista Henning Brand prvýkrát identifikoval prvok fosfor (P).
V nasledujúcom storočí, teda v 18. storočí, začali byť známe nové prvky, z ktorých najdôležitejšie boli plyny, a to vďaka rozvoju pneumatickej chémie vrátane kyslíka (O), dusíka (N) a vodíka (H).
Približne v tomto čase francúzsky chemik Antoine Lavoisier napísal zoznam jednoduchých látok, v ktorých sa už objavilo 33 prvkov.
Na začiatku devätnásteho storočia vynález elektrickej batérie spustil štúdium nových chemických javov, čo nakoniec prinieslo objav ďalších prvkov, ako sú alkalické kovy a kovy alkalických zemín.
Do roku 1830 už bolo identifikovaných 55 prvkov.
V polovici devätnásteho storočia sa pomocou vynálezu prístroja nazývaného spektroskop našlo viac prvkov, najmä tých, ktoré súvisia s farbou, ktorá predstavuje ich spektrálne čiary, vrátane cézia, tália a rubídia.
Spektroskop je prístroj, ktorý sa používa na pozorovanie a dosiahnutie spektra. Je to výsledok rozptylu série žiarenia, zvuku alebo vlnových javov.
Podobnosť, ktorú určité prvky predstavovali z hľadiska chemických a fyzikálnych vlastností, viedla vtedajších vedcov k tomu, že sa rozhodli ich systematicky usporiadať a zoskupiť podľa určitých kritérií.
Najodľahlejším predchodcom daného zákona je dobre známy Zákon o oktávach, ktorý vyvinul anglický chemik John Alexander Newlands, ktorý navrhol prebudenie ako veľkú novinku, že každých osem prvkov sa stretávame s podobnými vlastnosťami.
To bol preňho štart do formulovania vlastnej periodickej tabuľky formálne publikovanej v roku 1863.
Akoby jeden bol v postgraduách, rukavice v tomto zmysle si vzal iný chemik, v tomto prípade Nemec Julius Lothar Meyer, ktorý ako východiskový bod použil výsledky Newlands v roku 1870 a určil atómové objemy prvkov.
Keď spočítal atómové hmotnosti a predstavoval ich, bol schopný preukázať svetu vedy potvrdenie, že atómová hmotnosť znamená zvýšenie fyzikálnych vlastností.
A takmer súčasne s dielami Meyera, Ruský chemik Dimitri Mendeleev zverejňuje prvá periodická tabuľkaPorazil Meyera, ktorý by to urobil o rok neskôr, a preto je to on, kto zostal zásluhou jeho tvorcu.
Mendelejev by usporiadal prvky v rastúcom poradí na základe atómovej hmotnosti, ktorú predstavujúMedzitým do rovnakého stĺpca umiestnil tých, ktorí zdieľali niektoré charakteristiky.
Za zmienku stojí, že do tejto doby bolo známych už 63 prvkov z 90 existujúcich.
Tabuľka bola na konci 19. storočia doplnená ďalšou skupinou nazývanou nula, ktorá bola tvorená vzácnymi plynmi.